Las sustancias naturales son aquellas que se encuentran en la naturaleza, mientras que, las sustancias sintéticas son aquellas que hacemos los seres humanos, como la fabricación de medicamentos o pesticidas o la obtención de metales puros.
Diferentes tipos de reacciones son:
- Reacciones de oxidación - reducción: Una reacción de reducción es cualquier proceso en el que un compuesto pierde oxígeno y una oxidación en el que lo gana.

- Reacciones de combustión: Es la oxidación de un combustible en presencia de aire.
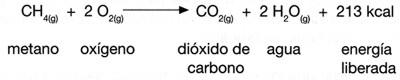 La energía liberada se desprende en forma de calor y luz (fuego).
La energía liberada se desprende en forma de calor y luz (fuego).- Reacciones de neutralización: Son aquellas en las que reacciona un ácido con una base para dar una sal y agua. Por ejemplo para la producción de jabones, en los que un ácido graso se neutraliza con Hidróxido de sodio o potasio.

- Reacciones de polimerización: Es un proceso por el que los monómeros se unen entre si para formar un polímero. Un monómero es una molécula sencilla que se une como los eslabones de una cadena.

Ejercicio 34
ResponderEliminarEn un alimento que cada 100g aporta 1876kJ:
22g son grasas y aportan 412,72kJ
42g son hidratos de cárbono y aportan 787,92kJ
17 g son fibra alimentaria y aporta 318,92kJ
13g son proteínas y aportan 243,88kJ
2,7g son sal y aportan 50,652kJ
Soy Ángela León.
ResponderEliminarEjercicio 8:
2Sn(s) + O2(g) = 2SnO(s)
S(s) + Hg(l) = HgS(aq) ya está ajustada.
2Fe(s)+ 3Cl2(g) = 2FeCl3(s)
C(s) + CO2(g) = 2CO(g)
4Al(s) + 3O2(g) = 2Al2O3(s)
Te(s) + H2O(l) = TeO(aq) + H2(g) ya está ajustada.
PdCl2(aq) + 2HNO3(aq) = Pd(NO3)2(s) + 2HCl(aq)
Hola doy Lucía Polo y este es el ejercicio 31
ResponderEliminara)2Cu + O2 = 2CuO DE OXIDACIÓN
b)CuO + H2 = Cu + H2O DE REDUCCIÓN
c)PbO2 + C = Pb + CO2 DE REDUCCIÓN
d)2Zn + O2 = 2ZnO DE OXIDACIÓN
e)Sn + O2 = SnO2 DE REDUCCIÓN
f)WO3 + 3H2 = W + 3H2O DE OXIDACIÓN
g)SnO2 + 2C = Sn + 2CO DE REDUCCIÓN
10) Los materiales necesitados son:
ResponderEliminarMatraz de erlenmeyer
Tubo de ensayo
Balanza